新しい潰瘍性大腸炎(UC)研究 ~特定の腸内細菌がマクロファージを攻撃する~
「特定の腸内細菌がマクロファージを攻撃する」という発見とFMTの可能性
潰瘍性大腸炎(Ulcerative Colitis:UC)は、原因が完全には解明されていない慢性の炎症性腸疾患です。
「免疫」「腸内細菌」「腸管バリア」が複雑に絡み合って発症することは分かってきましたが、「何が炎症のスイッチを入れているのか?」 は長年の大きな謎でした。
2024年11月、Science誌に掲載された最新研究が、この問いに重要な手がかりを与えました。
それは―
「UC患者の腸内に、マクロファージ(腸の免疫細胞)を狙って殺す毒素を出す細菌が観察され、その細菌(Aeromonas変異株)がいると、腸の炎症が悪化しやすくなる」という驚くべき内容ででした。
当院で行っている腸内環境治療(腸内フローラ移植/分子栄養学/生活習慣改善)とも深く関係するため、わかりやすくまとめてご紹介します。
■ 潰瘍性大腸炎と腸内細菌の関係
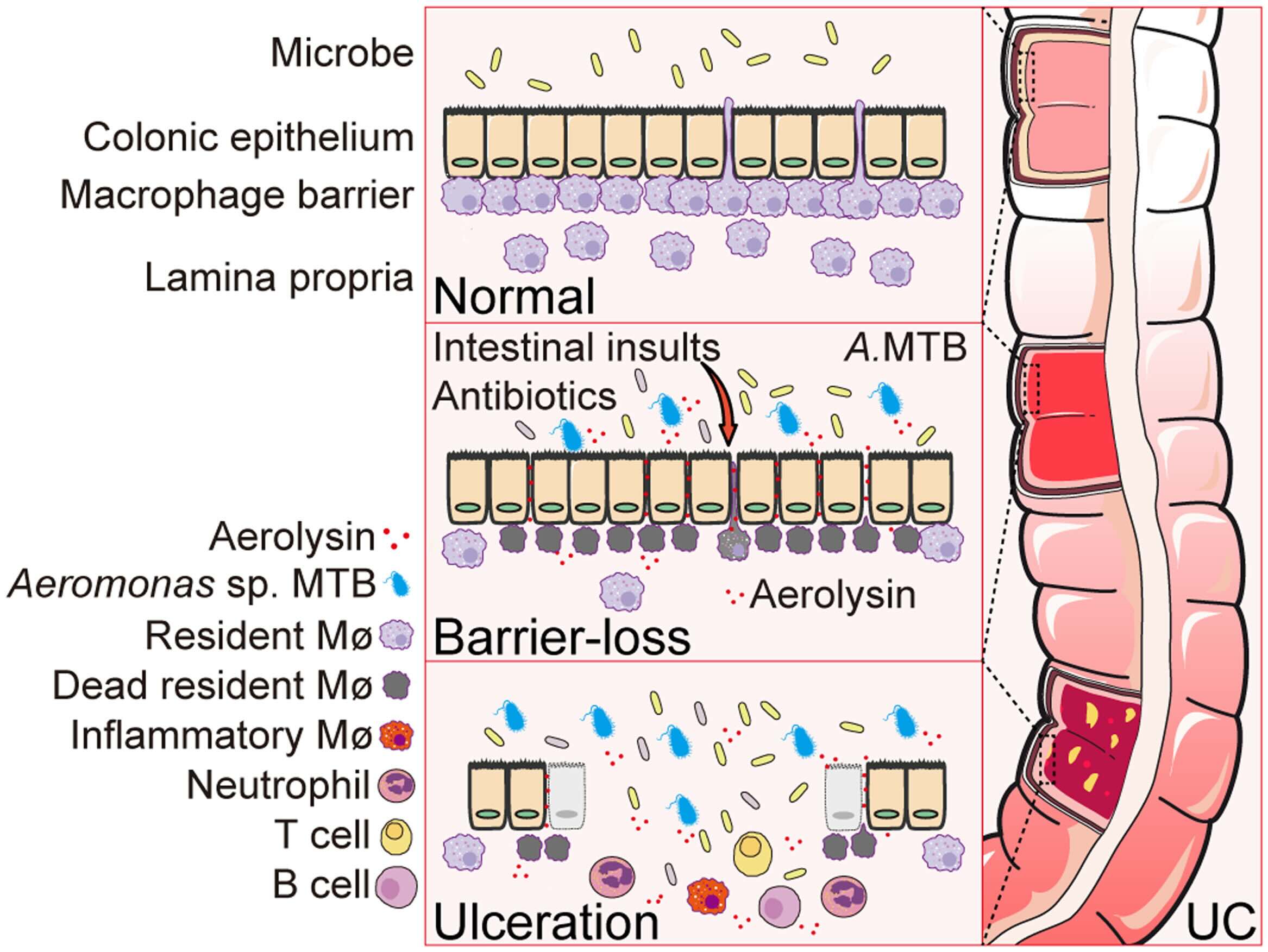
UCでは、腸の粘膜を守る「バリア」と、そのすぐ下で炎症の火消し役を担う「組織常在マクロファージ」が非常に重要です。
今回の研究では、
- ・UC患者の腸では、炎症が起きていない場所でもマクロファージが減っている
・そのマクロファージを“選択的に”殺す毒素(aerolysin)を出す細菌が見つかった
ことが示され、UCの発症メカニズムの一部が初めて“具体的に”描かれました。
■ 見つかったのは「Aeromonas」という細菌の変異株
研究チームはUC患者の腸粘膜を詳しく解析し、次のことを突き止めました。
① UC患者ではマクロファージが著しく減っている
しかも、炎症の有無に関係なく、粘膜のどの場所でも減少していました。これは「何かに攻撃されているのでは?」という強い示唆になります。
② その“攻撃者”は、ある細菌が出す毒素だった
検出されたのは Aeromonas という腸内細菌の変異株。この変異株は aerolysin(アエロリシン) という毒素を作り、マクロファージを選択的に死滅させます。
さらに興味深いのは、
- ・上皮細胞(腸管バリア)はあまり傷つけない
- ・マクロファージだけを狙い撃ちする
という点です。
③ マウスでの検証で因果関係が確認
毒素を出す株を腸内に入れたマウスでは、
- ・マクロファージが消失
- ・大腸炎が重症化
が確認されました。
一方、毒素を出さない株では炎症はほぼ起きませんでした。
④ UC患者ではその細菌が72%で見つかった
574人を対象とした解析では、
- ・UC患者:約72%でAeromonas陽性
- ・健常者:約12%
- ・クローン病:ほぼ検出されず
という明確な差がありました。つまりUCの背景には、「毒素を出す細菌がマクロファージを破壊し、腸の炎症を促す」というメカニズムが存在している可能性が高い、ということです。
■ では、なぜこの菌が増えるのか?
ここについてはまだ完全な答えはありません。
- ・食生活
- ・ストレスや睡眠
- ・抗生物質の既往
- ・腸のバリア機能低下
- ・ほかの腸内細菌との競争
- ・遺伝的要因
など、複数の因子が関わっていると考えられています。
当院が大切にしている「腸の粘膜修復」「マクロファージ含む免疫細胞の回復」「腸内細菌叢の再構築」といったアプローチは、この研究にも完全に一致しています。
■ この研究から導かれる“新しい治療の方向性”
今後、以下のような治療が開発される可能性があります。
・ Aeromonas変異株やaerolysin毒素を検出する検査
→ UCのリスク評価や再燃予測に活用できる可能性
・Aeromonasの定着を防ぐ腸内細菌治療
→ FMTや次世代プロバイオティクスの方向性として期待
・マクロファージを保護・回復させる治療
→ 栄養療法、生活習慣改善、免疫栄養の重要性がより高まる
・毒素をブロックする分子標的治療
→ 新規UC治療薬につながる研究も進むでしょう
■ 当院としての視点
当院では、
- ・腸粘膜の修復
- ・腸内細菌叢の再構築(FMT)
- ・マクロファージを含む免疫代謝の改善(分子栄養)
- ・ストレスケア(心身医療・サイモントン療法)
など、UCの「背景にある根本プロセス」を丁寧に診ています。
今回の研究は、「腸内細菌と免疫細胞の壊れたバランスを整える」という当院の治療コンセプトが、科学的にも非常に理にかなっていることを裏づける内容でした。
特に、FMTではこうした“有害株の除去・置換”が期待できるため、今後さらに有望な治療選択肢として位置づけられていくと思われます。